 万唯使命 让中考教学更高效,助力教育公平
万唯使命 让中考教学更高效,助力教育公平
只做中考
中考研究院
服务全国28省区
年超4600万人次的选择
万唯诞生
中考研究院
师生的选择
20年来,万唯专注研究中考、高考及PISA等试题
专人专职实时搜集适合命题的素材
构建起庞大的命题素材库
每年研发高品质原创题超20万道
使每本万唯图书不重题
老师说“万唯题好”:
素材新,情境真实,一题多设问
将“中考新考法”融入原创题
助力师生把握中考趋势、高效备考
万唯以“命题即教学”理念盘点各地名师实操备考法
组织名师主题教研交流,提升教学质量
2017年以来开设1300余场公益备考会
万唯,用千人研究院支持老师的备考教学
全国视野,原创题好
年超4600万人次的选择
更多名校,总复习从《试题研究》开始

20年来,万唯中考每进入一个新的省区,都带来持续热销和震动,河北、江西、天津、福建......无不如此。
随着专版区域越来越多,内容不断创新升级,“中考原创好题用万唯”的全国共识日益深入。截至2024年,万唯已服务28省区,这也成为万唯中考独具全国视野优势的原因。
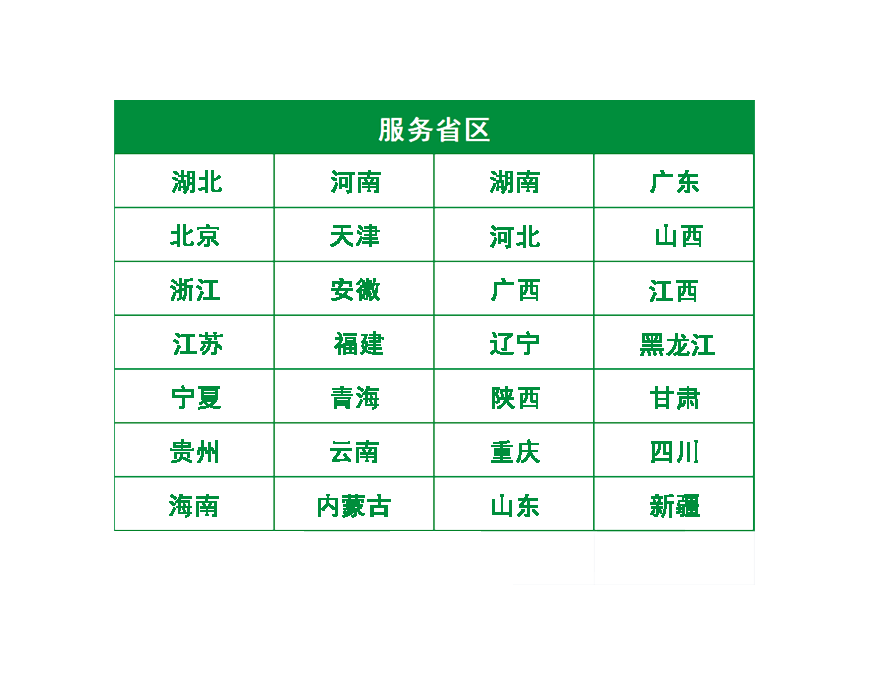
20年来,万唯中考每进入一个新的省区,都带来持续热销和震动,河北、江西、天津、福建......无不如此。
随着专版区域越来越多,内容不断创新升级,“中考原创好题用万唯”的全国共识日益深入。截至2024年,万唯已服务28省区,这也成为万唯中考独具全国视野优势的原因。




